胆烷酸偶联乙二醇壳聚糖包覆的PLGA纳米微球用于胰岛素口服递送的研究获进展
发布时间:2021-12-02
糖尿病是一种常见的由胰岛素分泌不足或胰岛素抵抗引起的慢性代谢性疾病,全世界有数亿人患此疾病,且确诊人数逐年上升,因此,其已成为全球公共卫生面临的最大挑战之一。皮下注射胰岛素是目前治疗1型糖尿病和晚期2型糖尿病最常用的方法,但其存在诸如低血糖、脂肪萎缩、注射疼痛、使用不便等缺点,导致患者的依从性很差。目前临床上亟需研发一种无痛、方便、可口服给药的胰岛素口服制剂。然而,胰岛素作为一种蛋白质药物,因为胃肠道的酸和酶屏障以及肠道上皮细胞的低摄取,导致其直接口服药效很差。
针对以上挑战,中国科学院苏州纳米技术与纳米仿生研究所张智军研究员团队与中国药科大学金亮教授团队密切合作,设计、制备了一种具有良好酸稳定性的壳聚糖包覆的PLGA微球GC-CA@ PLGA NPs。在此工作中,胰岛素被包覆在PLGA内部,可以免受酸和酶的降解,而表面修饰的乙二醇壳聚糖则提供了正电性与亲水性,一方面提高微球在肠道的摄取,另一方面可以实现在血液中的长效释药,从而达到口服长效平稳降糖的效果。研究人员还通过在GC上接枝疏水支链5-β胆烷酸(CA),显著提高了载药微球在胃酸中的稳定性(图1)。经过以上包封与修饰,载胰岛素微球GC-CA@ PLGA NPs表现出优异的稳定性,在口服给药时显示出更强、更长效的降糖效果。用肠道上皮细胞模型研究发现,相比较未偶联胆烷酸的GC @ PLGA NPs,实验组微球在模拟胃酸消化后表现出更高的细胞摄取效率(图2)。在此基础上,通过糖尿病小鼠模型的建立,发现载胰岛素的GC-CA@ PLGA NPs表现出长达24 h的降糖效果,口服生物利用度可达30%,相较于两组对照组微球分别提升了251%和106%(图3)。
上述工作为口服蛋白质多肽类药物的研发提供了一种新的策略。相关研究成果以“Improved oral delivery of insulin by PLGA nanoparticles coated with 5β-cholanic acid conjugated glycol chitosan”为题,近期发表在国际学术期刊Biomedical Materials上。
中科院苏州纳米所与中国药科大学联培硕士生王伟志为第一作者,张智军研究员和金亮教授为共同通讯作者。
Weizhi Wang, Chenggong Yu, Fangfang Zhang, Yuxuan Li, Bo Zhang, Jie Huang, Zhijun Zhang* and Liang Jin* Biomed. Mater., 2021, 16, 064103.
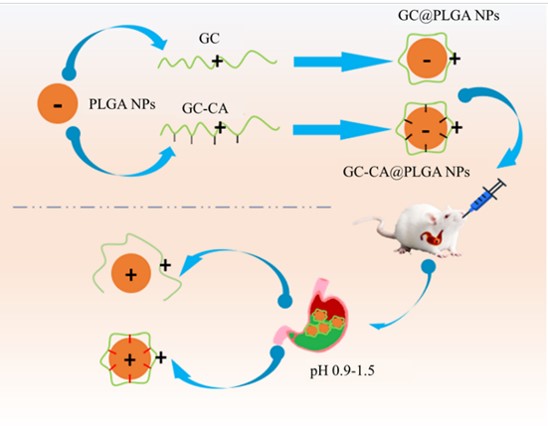
图1. 用于胰岛素口服递送的GC-CA@ PLGA NPs的制备及其抵抗胃酸的原理示意图。

图2. 激光共聚焦显微镜拍摄的Caco-2细胞对五种不同微球的摄取效果,bar = 50 μm。
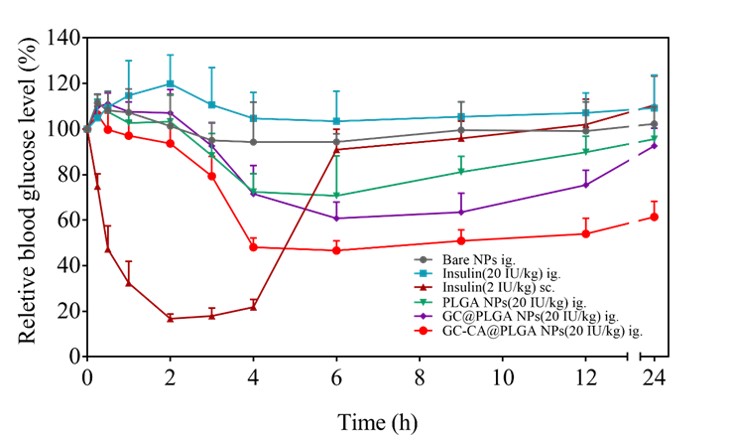
图3. 不同组别糖尿病小鼠给药后的血糖变化曲线。