涡旋磁性纳米环标记移植间充质干细胞用于体内肝纤维化治疗与MRI示踪研究取得进展
2022-03-21
肝纤维化是一种复杂的纤维化和炎症过程,由慢性肝损伤引起,是肝硬化发展的早期阶段。在肝纤维化过程中,富含胶原蛋白I和III的细胞外基质(ECM)持续积累会导致瘢痕沉积和肝纤维化加重。如果不及时治疗,会逐渐发展为肝硬化,同时肝细胞癌的风险也会增加,最终将导致器官衰竭而死亡。肝移植目前被认为是晚期肝病的唯一治疗方法,但其受限于供体短缺,价格昂贵以及免疫反应等问题。间充质干细胞(MSCs)在治疗肝纤维化方面具有显著效果,有望代替肝移植成为一种安全有效的肝纤维化治疗策略。对移植MSCs进行长期无创体内示踪对于阐明MSCs在肝纤维化治疗过程中的作用机制至关重要。但干细胞的增殖与胞吐作用会阻碍示踪剂在细胞内长期保留,使干细胞内示踪剂含量快速被稀释到检测限以下,阻碍了干细胞的长时程有效示踪。因此通过提高示踪剂的弛豫率和标记效率来延长示踪时间对于干细胞体内示踪具有重要意义。
针对以上肝纤维化临床治疗现状及挑战,本课题组与西北大学樊海明教授密切合作,设计、制备了一种基于亚铁磁涡旋氧化铁纳米环(FVIO)的纳米示踪剂,用于肝纤维化小鼠体内移植MSCs长期磁共振成像(MRI)可视化跟踪(图1)。如图2所示,我们设计、制备的FVIO@PEG纳米示踪剂的T2*弛豫率是商用造影剂的13倍左右,相同Fe浓度下也展现出更高的MRI对比度。实验发现,利用FVIO@PEG纳米示踪剂能够实现对移植MSCs连续28 天的体内MRI监测,同时考察了移植MSCs在体内的迁移归巢行为(图3)。在此基础上,研究人员还探讨并初步阐明了FVIO@PEG标记的MSCs在改善肝纤维化的机制,包括减少炎症和氧化应激、抑制肝纤维化引起的组织病理学损伤,以及下调相关细胞因子的表达。该工作能够加深我们对MSCs在肝纤维化治疗中的行为和作用的理解,推动干细胞在肝病治疗中的临床应用。
上述成果近期在线发表在国际学术期刊Nanoscale上。中科院苏州纳米所与上海大学联培硕士生王宇洁为第一作者,课题组张智军研究员,黄洁副研究员以及西北大学樊海明教授为共同通讯作者。该工作得到国家重点研发计划(2017YFA0104301)、国家自然科学基金(81801769)、中科院国际合作项目(121E32KYSB20200021)等项目的资助。
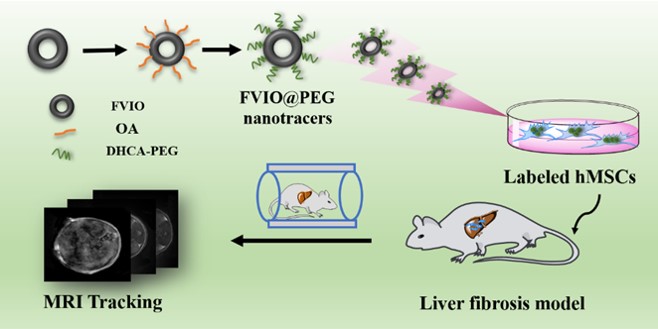
图1. FVIO@PEG纳米示踪剂的制备及其用于肝纤维化小鼠体内移植MSCs的MRI示踪示意图。
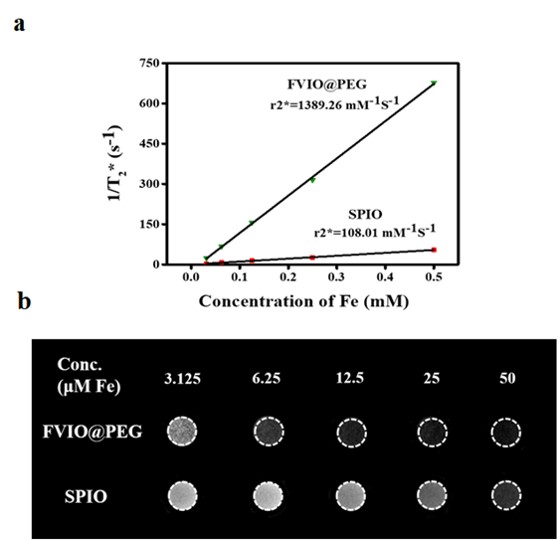
图2. FVIO@PEG和商用MRI造影剂SPIO在不同Fe浓度下的T2*弛豫率和T2*加权MR图像。
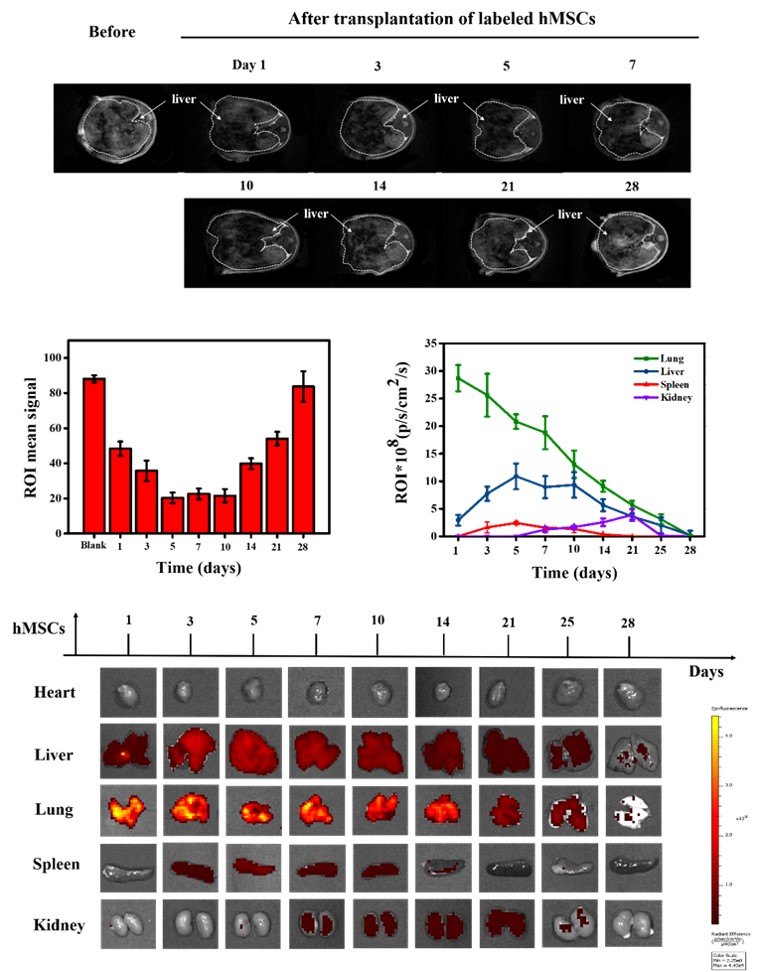
图3. 体内MR成像及MSCs体内分布。