生物3D打印构建导电水凝胶神经支架用于脊髓损伤修复的研究取得进展
2023-03-22
以神经干细胞(neural stem cells, NSCs)移植为代表的再生医学技术为脊髓损伤(spinal cord injury, SCI)等中枢神经疾病的临床治疗提供了一种前瞻性方案,然而,由于缺乏细胞外基质的支撑,移植干细胞在病灶部位难以专一地向神经元分化,极大地限制了干细胞移植的治疗效果与临床转化。
随着组织工程学的不断发展,利用生物3D打印技术构建具有脊髓仿生结构的水凝胶神经支架作为移植NSCs的载体,为提高移植NSCs的功能与疗效提供了一种可行的方式。一般认为,神经支架的理化性质与NSCs的行为、命运密切相关。研究表明,具有良好导电性的水凝胶支架能够促进NSCs的增殖、迁移及分化,因而有利于加速神经损伤的再生修复。尽管导电水凝胶支架在神经组织工程领域具有较好的应用前景,但其在NSCs移植及功能调控方面的应用依然缺乏系统深入的研究。
近年来,中科院苏州纳米所张智军研究员团队在生物3D打印神经组织工程支架等方面取得了系列进展(Biomaterials 2020, 272, 120771; Macromolecular Bioscience 2022, 22, 2200181; Acta Biomaterialia 2022, 151, 148-162; Chemical Engineering Journal 2023, 451, 138788)。近期,该团队针对SCI治疗过程中移植NSCs向神经元分化效率低等问题,合成了一种水溶性导电聚合物PEDOT:CSMA,TA,利用生物3D打印技术构建了一种负载NSCs的导电水凝胶支架。细胞实验表明,PEDOT:CSMA,TA的掺杂显著地促进了支架内部NSCs向神经元的定向分化(Biomaterials Advances 2022, 133, 112639)。在此基础上,研究人员考察了导电水凝胶支架植入在大鼠全横断SCI疾病模型上的治疗效果(图1)。研究表明,导电水凝胶支架能够通过促进神经突起的生长、加速胞外Ca2+内流,增强支架内部NSCs的细胞间通讯(图2)。经植入体内后,导电水凝胶支架显著抑制了病灶部位星形胶质细胞的生长以及瘢痕组织的沉积,延缓脊髓组织纤维化进程,进而提高了移植NSCs在SCI修复过程中的治疗效果(图3)。
上述研究以“Inhibited astrocytic differentiation in neural stem cell-laden 3D bioprinted conductive composite hydrogel scaffolds for repair of spinal cord injury”为题,近期在线发表于国际学术期刊《Biomaterials Advances》上,苏州纳米所2022届博士毕业生宋少帅为论文第一作者,张智军研究员和黄洁副研究员为共同通讯作者。研究工作得到了中科院战略性先导专项(XDA16020100)和苏州市基础研究试点项目(SJC2021011)的资助。
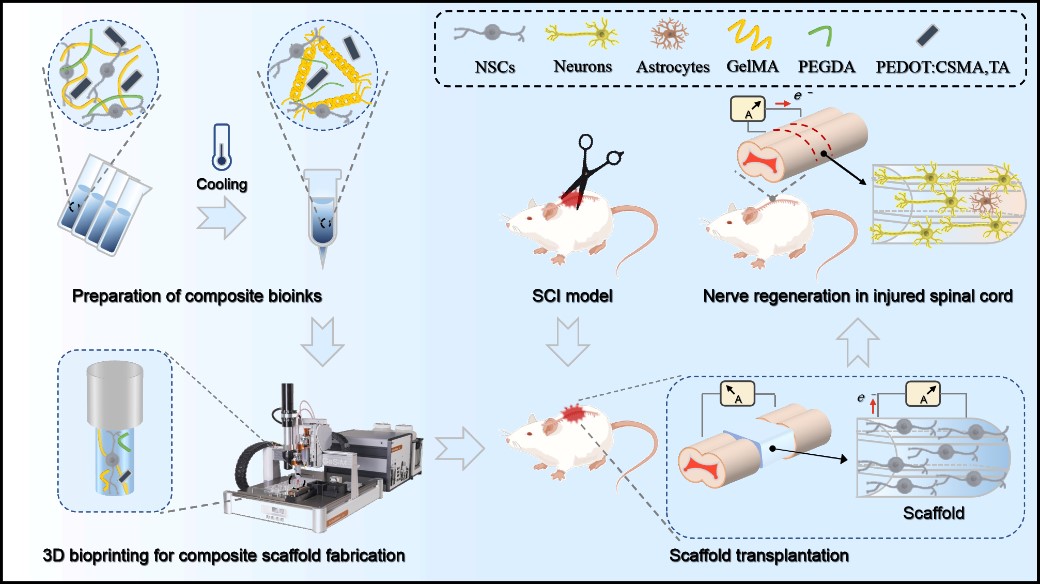
图1. 生物3D打印构建导电水凝胶神经支架用于脊髓损伤修复的示意图。

图2. 3D打印导电水凝胶支架的体外实验研究:(A) 导电水凝胶支架的全貌 (B) 3D打印支架的形状保真度 (C) 支架的体外稳定性 (D) GP水凝胶支架内部NSCs的形态 (E) GPP-TA导电水凝胶支架内部NSCs的形态 (F) 支架内部NSCs的胞内Ca2+荧光成像 (G) 神经突起平均长度与胞内Ca2+平均荧光强度的统计分析结果。

图3. 负载NSCs的导电水凝胶支架修复脊髓损伤的实验结果: (A) 动物实验流程, (B) SCI大鼠运动功能BBB评分, (C) 免疫荧光标记神经细胞再生情况。
论文信息:S. Song, Y. Li, J. Huang*, S. Cheng, Z. Zhang*. Inhibited astrocytic differentiation in neural stem cell-laden 3D bioprinted conductive composite hydrogel scaffolds for repair of spinal cord injury [J]. Biomaterials Advances, 2023, 148, 213385.
原文链接:https://doi.org/10.1016/j.bioadv.2023.213385